近期,我校3044am永利集团3044noc余晓斌教授团队在连续可控制备目标聚合度壳寡糖方面取得重要进展,研究成果“Engineering of a chitosanase fused to a carbohydrate-binding module for continuous production of desirable chitooligosaccharides”正式发表于Carbohydrate Polymers (IF=9.381) (https://doi.org/10.1016/j.carbpol.2021.118609)。
聚合度为3-7的壳寡糖具有更好的生物活性,而酶法降解壳聚糖制备壳寡糖的聚合度通常为2-4。酶的工业化应用的关键是固定化,但繁琐、费时费力的酶纯化过程、昂贵的载体、有毒有机化合物的引入及酶自身的不稳定性仍然是限制酶固定化工业应用的主要瓶颈。
在该研究中,研究人员前期筛选到来自烟曲霉Aspergillus fumigatus CJ22-326的壳聚糖酶,其具有不能切割壳二糖、壳三糖和壳四糖,并且很难切割壳五糖的特点。通过在Csn75的C端融合来源于嗜盐芽孢杆菌(Bacillus halodurans)的β-(1,3)-葡聚糖酶的可特异性亲和热凝胶多糖的碳水化合物结合结构域(Carbohydrate Binding Module,CBM),获得了具有“结合”和“催化”双功能的融合酶Csn75-CBM。一步纯化、固定化制备了热凝胶多糖壳聚糖酶填充床反应器(Chitosanase Immobilized Curdlan Packed-Bed Reactor,CICPR)。通过控制酶的加载量、底物浓度和流速,利用CICPR制备了DP分别为:2-5、3-6和3-7的壳寡糖,相应的水解率分别为:97.75%、75.45%、75.45%。采用每4 h补料Csn75-CBM粗酶液实现原位CICPR更新,使水解产物中壳寡糖稳定产出。
余晓斌教授为论文通讯作者,3044am永利集团3044noc博士生周剑丽为第一作者。上述研究工作得到了国家轻工技术与工程一流学科(LITE2018-08)、3044am永利集团3044noc糖化学与生物技术教育部重点实验室2020开放课题:《融合CBM高效固定化壳聚糖酶用于壳寡糖的可控制备》(项目编号:KLCCB-KF202007)等项目资助。
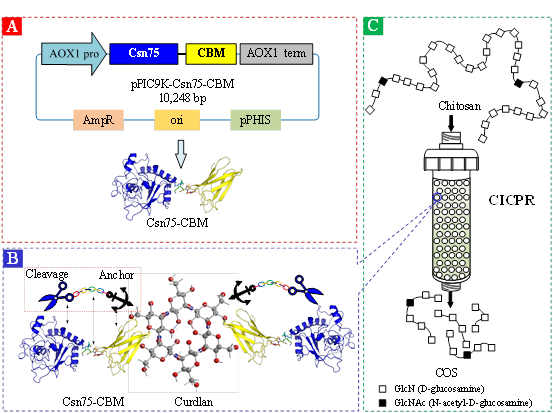
热凝胶多糖固定化壳聚糖酶填充床反应器示意图
